Aufgabenteilung bei Rezeptoren
Rund 800 verschiedene G-Protein-gekoppelte Rezeptoren sind im menschlichen Körper bekannt. Einen großen Teil davon stellen die Adhäsions-GPCRs dar: Sie sorgen unter anderem dafür, dass sich das Gehirn richtig entwickelt und hemmen das Wachstum von Metastasen und Melanomen. Mutationen in Adhäsions-GPCRs hingegen können zu angeborenen Krankheiten führen, die unter anderem zu einer geistigen Behinderung führen können. Trotz dieser wichtigen Funktionen wissen Forscher bisher nur wenig darüber, wie die Adhäsion GPCR arbeiten.
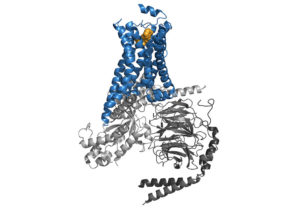
Die Arbeitsgruppe von Prof. Felix Engel aus der Nephropathologie am Universitätsklinikum Erlangen der FAU hat nun die Wirkungsweise eines bestimmten Rezeptors – dem GPR126 – der Adhäsions-GPCR-Familie untersucht. Dieser spielt sowohl eine Rolle bei der Entwicklung des Herzens als auch bei der Markreifung des peripheren Nervensystems. Das Ergebnis: GPR126 entfaltet seine Wirkung anders als bisher angenommen. Adhäsions-GPCRs besitzen eine einzigartige molekulare Struktur: Sie bestehen aus zwei Teilen, dem N-Terminus (NTF), der aus der Zelle hinausragt, mit der Zellumgebung bzw. benachbarten Zellen interagieren und Signale aufnehmen kann, und dem C-Terminus (CTF), der sieben Transmembrandomänen enthält, zur Verankerung in der Zellmembran, sowie einen Teil, der ins Zellinnere ragt und hier die Signale weiterleitet.
Adhäsions-GPCRs werden vor der Verankerung in der Zellmembran in NTF und CTF gespalten. Bisher waren Wissenschaftler davon ausgegangen, dass die Spaltung des Rezeptors für seine Funktion keine Rolle spielt. Professor Engel und sein Team haben nun gezeigt, dass jeder Teil spezifische Aufgaben übernimmt. Anhand von Versuchen am Modell wiesen die FAU-Forscher nach, dass nur das NTF – und nicht das CTF – eine wichtige Rolle bei der Entwicklung des Herzens spielt.
„Unsere Studie zeigt, dass GPR126 gewebe-spezifische Funktionen ausübt. Sie bietet ein einzigartiges Beispiel für die Signalübermittlungsmechanismen der Adhäsions-GPCRs in Wirbeltieren“, erklärt Prof. Engel. „Das ist eine Grundvoraussetzung um die physiologischen und pathologischen Funktionen von Adhäsions-GPCRs zu verstehen und dieses Wissen in der Zukunft in Medikamenten zur Behandlung von Erkrankungen zu nutzen.“
Weitere Informationen:
Prof. Felix Engel
Tel.: 09131/85-25699
felix.engel@uk-erlangen.de